Thông báo của FDA: Thuốc huyết áp bị thu hồi sau khi chất opioid mạnh được tìm thấy
Một nhà sản xuất cho biết họ đang bắt đầu thu hồi thuốc huyết áp của mình

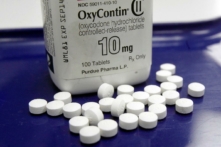
Theo thông báo của Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA), trong tuần này (02-07/10), một nhà sản xuất thuốc cho biết họ đang bắt đầu thu hồi thuốc điều trị huyết áp do sự hiện diện của chất opioid tổng hợp oxycodone.
Theo bản thông báo, hãng dược phẩm KVK-Tech cho biết họ đang thu hồi các viên betaxolol 10mg, được phân phối cho nhà bán lẻ và bán buôn trên khắp nước Mỹ.
Lô hàng này được thu hồi như một biện pháp đề phòng vì một viên oxycodone được tìm thấy trên dây chuyền đóng gói trong quá trình thông quan dây chuyền. Công ty cho biết họ chưa nhận được báo cáo nào về “viên thuốc ngoại lai” trong lọ betaxolol.
Thông báo thu hồi cho biết: “Gói betaxolol có dán cảnh báo về tác dụng làm chậm nhịp tim ở bệnh nhân cao niên, tình trạng này có thể trở nên trầm trọng hơn do opioid. Ngoài ra, một số bệnh nhân được kê betaxolol liều thấp có thể bị tổn hại chức năng tim phổi, tình trạng này cũng trầm trọng hơn khi bệnh nhân dùng opioid. Hơn nữa, viên betaxolol 10mg và viên oxycodone 5mg có sự khác biệt nhỏ về hình thức, khiến một người dùng viên betaxolol 10mg thường xuyên có thể không chú ý.”
Thông báo lưu ý rằng một số bệnh nhân khi dùng quá liều “có thể bị ảnh hưởng tiêu cực” bởi oxycodone, một chất gây nghiện mạnh.
Thông báo thu hồi cho biết thêm, điều đó thậm chí còn nghiêm trọng hơn nếu “một lượng lớn viên oxycodone có trong lọ betaxolol. Do vậy, việc vô tình tiếp xúc với một chất được kiểm soát, chẳng hạn như oxycodone, ở nhóm bệnh nhân này có thể dẫn đến tình trạng thở chậm đáng kể, hay suy hô hấp, là một nguy cơ nghiêm trọng cho sức khỏe.”
Các viên betaxolol được đóng gói trong lọ nhựa màu trắng với số lượng 100 viên và có hạn dùng đến tháng 06/2027. Số lô là 17853A.
KVK cho biết họ đã thông báo cho các nhà phân phối và khách hàng bằng thư thu hồi qua email và thư qua đêm vào ngày 27/09 và sẽ thu xếp việc trả lại sản phẩm bị thu hồi. Một số lượng nhỏ lọ thuốc chứa oxycodone có thể được phân phối cho các hiệu thuốc bán lẻ.
Thông báo cho biết những khách hàng đã mua thuốc sẽ được công ty hoàn trả chi phí, bổ sung thêm rằng nếu một người gặp vấn đề liên quan đến thuốc, họ nên liên hệ với bác sĩ hoặc nhà cung cấp dịch vụ chăm sóc sức khỏe.
Nếu có bất kỳ câu hỏi nào liên quan đến việc thu hồi, khách hàng có thể liên hệ với KVK theo số 215-579-1842, máy lẻ 6002, từ Thứ Hai đến Thứ Sáu, từ 8 giờ sáng đến 6 giờ chiều giờ miền Đông hoặc qua email tại [email protected].
Những lần thu hồi thuốc khác
Vài tuần trước, FDA thông báo rằng Marlex Pharmaceuticals đã tự nguyện thu hồi một lô Viên nén Digoxin USP 0.125mg và một lô Viên nén Digoxin 0.25mg USP.
Theo thông báo, lý do được đưa ra là do “nhầm nhãn,” có thể dẫn đến việc người bệnh dùng sai liều thuốc. Phiên bản thuốc trợ tim yếu hơn được đựng trong lọ ghi nhãn của thuốc mạnh hơn và ngược lại.
Thông báo cho biết: “Việc nhầm nhãn có thể gây ra tình trạng quá liều hoặc dưới liều ở bệnh nhân vô tình dùng sai. Những bệnh nhân có ý định dùng Digoxin Tablets USP … sẽ nhận được một liều cực mạnh và bị ngộ độc thuốc đáng kể (với các triệu chứng như mất phương hướng tâm thần, chóng mặt, mờ mắt, mất trí nhớ và ngất xỉu) khi vô tình dùng quá liều.”
Theo thông báo, “Sản phẩm này được dùng để điều trị bệnh suy tim nhẹ đến trung bình. Digoxin làm tăng co bóp cơ tim ở bệnh nhi bị suy tim. Digoxin được chỉ định để kiểm soát tốc độ đáp ứng tâm thất ở người trưởng thành bị rung nhĩ kinh niên. Sản phẩm được đóng gói dưới dạng 100 viên trong lọ HDPE màu trắng và được dán nhãn bên dưới với NDC, lô hàng và ngày hết hạn.”
Cùng thời gian này, FDA thông báo riêng về việc thu hồi viên nang WEFUN sau khi cơ quan phát hiện sản phẩm này bị nhiễm một loại thuốc khác là sildenafil.
“Phân tích của FDA phát hiện sản phẩm WEFUN bị nhiễm sildenafil. Sildenafil là một chất ức chế Phosphodiesterase (PDE-5) chứa trong các sản phẩm được FDA phê chuẩn để điều trị rối loạn cương dương ở nam giới. Sự hiện diện của sildenafil trong sản phẩm cho thấy đây là thuốc không được phê chuẩn, độ an toàn và hiệu quả chưa được thiết lập và do đó có thể bị thu hồi,” thông báo cho biết.
Thanh Ngọc biên dịch
Quý vị tham khảo bản gốc từ The Epoch Times