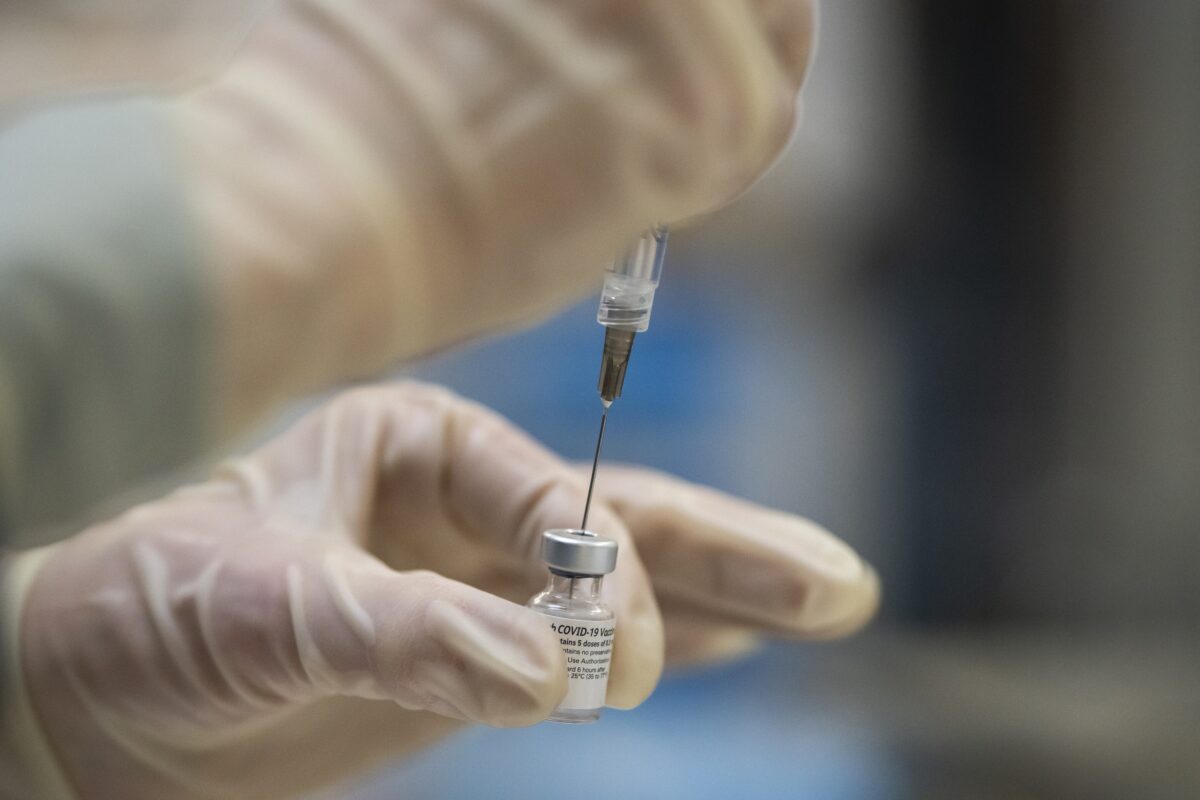
Pfizer, BioNTech xin FDA chấp thuận mũi vaccine COVID-19 mới cho trẻ sơ sinh và trẻ nhỏ

Hôm 05/12, Pfizer và BioNTech, một đối tác Đức của hãng Pfizer, đã thông báo rằng hai công ty này đã đề nghị các cơ quan quản lý Hoa Kỳ cấp phép cho mũi vaccine COVID-19 mới được cập nhật dành cho trẻ em từ 6 tháng tuổi của họ.
Hai công ty này muốn có giấy phép sử dụng khẩn cấp cho liều vaccine mới này, vốn sẽ được sử dụng như liều thứ ba trong phác đồ chích ngừa cho trẻ nhỏ giai đoạn từ 6 tháng đến 4 tuổi.
Những em nhỏ trên 4 tuổi hiện có thể được chích vaccine mới này dưới dạng một mũi tăng cường.
Mũi vaccine mới này chứa các thành phần của cả chủng virus Vũ Hán lẫn biến thể phụ BA.4/BA.5 của chủng Omicron. Vaccine cũ chỉ chứa biến thể virus Vũ Hán, loại biến thể vốn không còn lan truyền kể từ năm 2020.
Đơn yêu cầu cấp phép sử dụng trong trường hợp khẩn cấp (EUA), được nộp cho Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA), là dành cho một mũi 3 microgam. Mũi này sẽ là mũi thứ ba trong những gì được mô tả là phác đồ 3 mũi căn bản. Pfizer đã thêm mũi thứ ba vào phác đồ điều trị sơ khởi cho trẻ nhỏ sau khi hai mũi không kích hoạt được phản ứng miễn dịch đầy đủ. Phác đồ sơ khởi dành cho trẻ em từ 5 tuổi trở lên là hai mũi, và các mũi nhắc lại được gọi là các mũi tăng cường.
Pfizer và BioNTech cho biết trong một tuyên bố: “Khi các bệnh về đường hô hấp đang lan truyền ở trẻ em dưới 5 tuổi với mức độ cao, vaccine COVID-19 được cập nhật có thể giúp ngăn ngừa bệnh nặng và nhập viện.”
Không có bằng chứng lâm sàng để chứng minh cho tuyên bố đó.
FDA đã không phúc đáp một yêu cầu bình luận.
Hôm 31/08, cơ quan quản lý này đã cho phép loại vaccine thể lưỡng trị này (có sự kết hợp của biến thể gốc và biến thể Omicron) trở thành một mũi tăng cường cho những người từ 12 tuổi trở lên. Hôm 12/10, cơ quan này đã mở rộng giấy phép sử dụng khẩn cấp cho trẻ em từ 5 tuổi.
Cả hai hành động nói trên đều không dựa trên dữ liệu lâm sàng. Thay vào đó, cơ quan này đã trích dẫn dữ liệu tiền lâm sàng — thử nghiệm trên chuột — và dữ liệu từ một loại vaccine thể lưỡng trị khác không và chưa bao giờ được sử dụng tại Hoa Kỳ.
Cơ quan này cho biết trong một tuyên bố trước đó: “FDA xem dữ liệu đó là có liên quan và chứng minh rằng những loại vaccine này có chứa một thành phần của hai dòng biến thể phụ của Omicron là BA.4 và BA.5.”
Dữ liệu từ loại vaccine thể lưỡng trị BA.1/Vũ Hán cho thấy rằng vaccine này đã kích hoạt phản ứng miễn dịch tốt hơn so với vaccine cũ ở mũi thứ tư hoặc mũi tăng cường thứ hai. Dữ liệu này chỉ [được thu thập] từ những người tham gia trên 55 tuổi và không bao gồm các đánh giá về tính hiệu quả.
Thử nghiệm tiền lâm sàng trên chuột này cũng cho thấy lượng kháng thể trung hòa đã tăng vọt, được cho là một tín hiệu khả quan về khả năng bảo vệ chống lại COVID-19 khi so sánh với những mức độ mà vaccine cũ kích hoạt được.
Một phiên bản vaccine COVID-19 cập nhật của Moderna hiện sẵn có cho trẻ em từ 6 tuổi. Công ty này vẫn chưa yêu cầu EUA cấp phép cho loại vaccine cập nhật dành cho trẻ nhỏ. Cả vaccine Pfizer lẫn vaccine Moderna đều được xây dựng dựa trên công nghệ RNA thông tin (mRNA).
Dữ liệu duy nhất về tính hiệu quả của những loại vaccine mới này xuất phát từ Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh Hoa Kỳ (CDC). Cơ quan này nhận thấy những mũi chích mới này cải thiện khả năng bảo vệ chống lại nhiễm trùng có triệu chứng tuy nhiên khả năng bảo vệ đạt mức bằng hoặc dưới 50%.
Chuyên gia cho biết FDA không nên cấp phép
Việc cấp phép cho những loại vaccine cũ dùng cho trẻ nhỏ đã vấp phải sự phản đối mạnh mẽ vì trẻ em ít phải đối mặt với nguy cơ từ COVID-19 và những đánh giá về tính hiệu quả [của những loại vaccine cũ] không đạt tiêu chuẩn hoặc không đáng tin cậy. Xét đến việc thiếu dữ liệu lâm sàng, một số chuyên gia cũng đặt nghi vấn về việc cấp phép cho những mũi chích mới.
Tiến sĩ Harvey Risch, giáo sư danh dự về dịch tễ học tại Trường Y tế Công cộng Yale, cho biết những loại vaccine này không nên được cấp phép cho trẻ nhỏ, hơn nữa FDA không nên chấp thuận yêu cầu mới này.
Ông Risch nói với The Epoch Times trong một thư điện tử, “Ngay từ đầu, FDA đáng lẽ không bao giờ nên phê chuẩn vaccine mRNA để sử dụng chung cho nhóm tuổi này. Hiện thời FDA cũng không nên phê chuẩn loại vaccine mới này để sử dụng chung ở đây.”
Nhiều quốc gia đã phê chuẩn các loại vaccine COVID-19 được cải tiến vốn nhằm vào biến thể phụ BA.1 bên cạnh biến thể Vũ Hán, nhưng các cơ quan quản lý của Hoa Kỳ đã yêu cầu các nhà sản xuất vaccine nhanh chóng chuyển thành phần BA.1 sang thành phần BA.4/BA.5. Lý do đưa ra là những biến thể phụ đó đang trở nên chiếm ưu thế hơn ở Hoa Kỳ.
Hai biến chủng khác, BQ.1 và BQ1.1., đang ngày càng vượt lên BA.4 và BA.5. Theo dữ liệu của CDC, tính đến hôm 12/11 ở Hoa Kỳ, hai chủng BQ.1 và BQ1.1. chiếm 35.3% các ca nhiễm so với 46.7% của BA.4 và BA.5. Dựa trên phân tích mô hình, cơ quan này dự đoán số ca nhiễm BQ.1 và BQ1.1 sẽ tăng vọt lên 62.8% tính đến hôm 03/12, và các chủng khác giảm xuống chỉ còn 13.8%.
Trước đó, Tiến sĩ Risch đã cảnh báo rằng biến thể của virus sẽ thay đổi, điều mà ông nói sẽ khiến mũi tăng cường mới này trở nên lỗi thời.
CDC
Trong một hướng dẫn về kế hoạch hoạt động gần đây (pdf), CDC cho biết rằng loại vaccine thể lưỡng trị này sẽ sẵn có cho trẻ nhỏ vào tháng Mười Hai, đang chờ FDA cấp phép.
Cơ quan này cho biết, “Tại thời điểm này, dự kiến trẻ em trong các nhóm tuổi này sẽ được yêu cầu chích hai liều vaccine COVID-19 thể đơn trị trước khi chích một liều vaccine COVID-19 thể lưỡng trị.”

 Mới nhất
Mới nhất
 Tiêu điểm
Tiêu điểm
 Bình luận
Bình luận
 Email
Email